Un des points clés économiques des futures batteries au Lithium-Ion pour véhicules électriques ou hybrides rechargeables est d’éviter de mettre en oeuvre, dans leur électrode positive, des produits à base de métaux onéreux tels que le Cobalt ou le Nickel. En effet une batterie de 16 kWh constituée de 88 éléments d’accumulateur de 50Ah (exemple de la i-MIEV) comportera dans les 30 kg de matière électroactive. Parmi les matériaux possibles il faut donc proscrire le LiCoO2 très utilisé dans les petites batteries, il faut éviter le LiNiO2 lui aussi trop cher, on pourra accepter le LiMn2O4 en raison du faible coût du Manganèse mais le matériau idéal, d’un point de vue économique, serait sans nul doute le LiFePO4 (phosphate de Fer lithié). Mais ce produit présente la désagréable propriété de présenter un vieillissement intempestif en charge et en décharges rapides qui sont les régimes électriques privilégiés lors d’un freinage avec forte récupération d’énergie ou d’une accélération subite d’un véhicule. Les laboratoires japonais travaillent donc activement sur des formes nanométriques (20 à 40 nm de diamètres) enrobées de 1 à 2 nm de carbone de type semi-graphite (FIG.) qui permettent de mieux répartir les densités de courant au sein du matériau comme le montrent les petits électrons roses de la figure b. 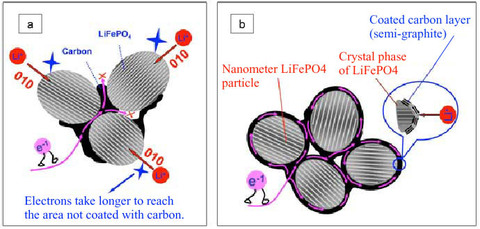
C’est l’Institut National of Advanced Industrial Science and Technology japonais (AIST) associé à la Japan Society For the Promotion of Science (JSPS) qui travaille sur ce sujet. On est là dans la démarche typiquement japonaise, les recherches amont sont diffusées et partagées par tous les acteurs du Marché, il leur appartiendra par la suite de développer et d’industrialiser leur propre solution avec leur sous-traitant. L’AIST a donc réussi à synthétiser des nanoparticules de LiFePO4 de structure olivine de 20 à 40 nm de diamètres enrobées d’une fine couche de semi-graphite obtenue par décomposition d’un coating organique. Bien sûr tout est dans le tour de main pour enrober chacune des nanoparticules au bon moment de leur croissance, avant qu’elles ne s’agrègent entre elles et de carboniser le dépôt organique à température suffisamment basse pour éviter le grossissement des grains. Le procédé doit être très pointu.
Ce revêtement poreux de carbone (loupe de la Figure b) permet de réduire la distance de déplacement des ions Li+ au sein du cristal et s’affranchit également de la faible conductivité électrique de ce produit. L’AIST revendique de pouvoir charger ou décharger ce matériau aux régimes de 30C ou 60C sans détérioration des caractéristiques et de pouvoir réaliser 1100 cycles à 100% de charge sans perte de la capacité initiale de 165 mAh par gramme.
Nul doute qu’en ce moment plein de chimistes japonais refont les recettes de l’AIST en les perfectionnant et en essayant de les rendre industrielles. L’enjeu est de taille!
Le 29 Août 2008
–

Laisser un commentaire