Que ce soit pour apporter de l’hydrogène à une pile à combustible ou mieux pour constituer le produit réducteur régénérable d’une pile à circulation en solvant organique, une des voies prometteuses des batteries du futur, le couple Al/AlH3 constitue un candidat intéressant. Dans un système électrochimique à définir sur une électrode l’hydrure d’Aluminium est oxydé en Aluminium, sur l’autre polarité de l’oxygène par exemple est réduit ces deux réactions électrochimiques libèrent une énergie considérable qui va permettre de propulser un véhicule électrique. La recharge de l’ensemble consistera à vidanger la solution usagée contenant l’Aluminium en suspension et à la remplacer par une solution neuve contenant de l’hydrure. Il reste alors dans une unité de traitement d’isoler l’Aluminium en poudre et de le transformer en hydrure. C’est sur cette phase du processus que Ragaiy Zidan vient de déposer un intéressant brevet à la suite des travaux de l’inventeur et de son équipe au sein du Savannah River Research Laboratory du DOE américain.
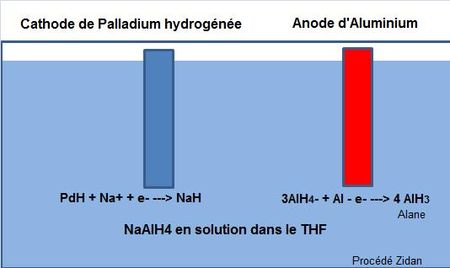
L’hydrure d’aluminium est obtenu par oxydation électrochimique du NaAlH4 (hydrure d’aluminium sodium) en solution dans le THF. L’oxydation de l’anion AlH4– sur une anode d’aluminium conduit à l’hydrure, alors que la réduction du Na+ sur une cathode de Palladium hydrogéné conduit à l’hydrure de sodium NaH (FIG.). Après utilisation de l’alane AlH3 et récupération de l’Aluminium, le NaH sera utilisé pour synthétiser à nouveau du NaAlH4 en présence d’hydrogène et d’un catalyseur à base de Titane.
NaH + Al +3/2 H2 ——-Ti ——> NaAlH4
Est ainsi défini un procédé en boucle pour obtenir l’AlH3 à partir de l’Aluminium, via l’intermédiaire de l’hydrure d’aluminium sodium.
LIRE le brevet de Zidan
Le 7 Juillet 2009

Laisser un commentaire